黄铜中铜质量分数的测定与分析
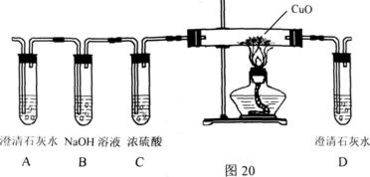
黄铜作为一种常见的铜锌合金,因其良好的机械性能、耐腐蚀性和美观的色泽,被广泛应用于电器零件及日用品制造中。测定黄铜中铜的质量分数,对于控制产品质量、优化材料性能具有重要意义。本次实验通过化学反应法,对一份黄铜样品中的铜质量分数进行了测定。
实验原理
黄铜中仅锌能与稀硫酸发生置换反应,生成硫酸锌和氢气,而铜不与稀硫酸反应。反应方程式为:
Zn + H₂SO₄ → ZnSO₄ + H₂↑
通过测量反应前后总质量的变化,可以计算出反应生成氢气的质量,进而推算出样品中锌的质量,最终求出铜的质量及其质量分数。
实验数据与计算
已知:
- 黄铜样品质量:10.0 g
- 加入稀硫酸质量:98.0 g
- 反应后烧杯中物质总质量:107.9 g
1. 计算生成氢气的质量
根据质量守恒定律,反应前总质量 = 黄铜样品质量 + 稀硫酸质量 = 10.0 g + 98.0 g = 108.0 g。
反应后总质量 = 107.9 g。
反应前后质量减少的部分即为逸出氢气的质量。
氢气质量 = 108.0 g - 107.9 g = 0.1 g。
2. 计算样品中锌的质量
设样品中锌的质量为 \( m{Zn} \)。
根据化学方程式:
Zn + H₂SO₄ → ZnSO₄ + H₂↑
65 g Zn 对应生成 2 g H₂。
即:
\[ \frac{m{Zn}}{65} = \frac{0.1}{2} \]
解得:
\[ m_{Zn} = \frac{65 \times 0.1}{2} = 3.25 \text{ g} \]
3. 计算样品中铜的质量及质量分数
铜的质量 = 样品总质量 - 锌的质量 = 10.0 g - 3.25 g = 6.75 g。
铜的质量分数 = \( \frac{6.75}{10.0} \times 100\% = 67.5\% \)。
结果与讨论
本次测定得出,该黄铜样品中铜的质量分数为67.5%,锌的质量分数为32.5%。此组成属于常见黄铜(如三七黄铜)的范围,具有良好的综合性能,适合用于制造对强度、延展性及耐腐蚀性有一定要求的日用品和电器零件。
在金属日用品制造中,黄铜的应用十分广泛。例如:
- 装饰五金:如门把手、锁具、灯具配件等,利用其金黄色的光泽和耐锈蚀特性。
- 厨具与餐具:部分高档水龙头、酒器、装饰性餐具采用黄铜制造,常进行表面镀铬或镍处理以增强耐用性和卫生性。
- 乐器与工艺品:如萨克斯管、号等管乐器,以及雕塑、奖牌等工艺品,利用其优异的声学性能和易加工性。
- 电器零件:如插头、插座触点、散热器等,利用其良好的导电性和导热性。
实验意义与注意事项
本实验方法简单、原理清晰,通过基础的化学定量分析即可获得合金组成。在实际工业生产中,控制黄铜中铜锌比例是调整其硬度、强度、塑性及耐腐蚀性的关键。例如,含铜量较高的黄铜(如65%-70%)更柔软、延展性更好,适合冷加工;而含锌量增高则会提高强度和硬度,但脆性也可能增加。
需要注意的是,实验中假设稀硫酸足量且反应完全,所有氢气均逸出并被准确计量。实际操作中需确保反应完全,并考虑环境因素对称量的影响,以提高测定精度。黄铜中可能含有少量其他元素(如铅、锡、铝等),对于更高精度的成分分析,可能需要借助光谱分析等仪器方法。
综上,化学分析法为理解合金组成提供了一种直观的手段,而黄铜作为一种经典合金材料,其成分与性能的关联性,持续支撑着它在日用品制造及工业领域中的重要地位。
如若转载,请注明出处:http://www.dezhitrede.com/product/69.html
更新时间:2026-05-28 10:02:00








